Meninos em células imunes impedem a capacidade do cérebro de limpar as placas de Alzheimer
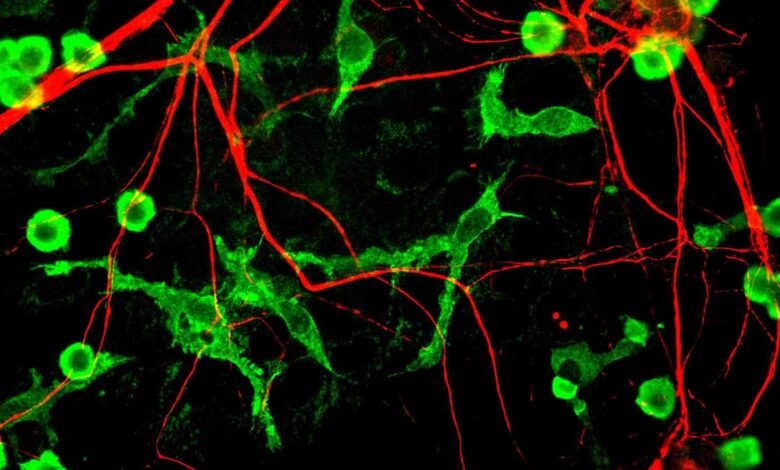
A doença de Alzheimer é um distúrbio cerebral gradual e Uma forma de demência Isso afeta a memória, o pensamento e o comportamento. Como os sintomas se tornam mais graves, a doença pode afetar seriamente a capacidade de uma pessoa de executar tarefas que podem ser consideradas rotina, como escovar os dentes, refeições ou até mesmo identificar membros da família.
Por muitos anos, a teoria líder foi que a doença de Alzheimer ocorre quando foi chamada de protenan prejudicial Beta e Yau Ameloid Regras no cérebro. Essa interconexão distingue uma série de eventos, finalmente prejudicando as células nervosas e levando à perda de memória, confusão e mudanças de humor. Essa destruição não ocorre da noite para o dia. Começa anos, mesmo antes que os sintomas apareçam.
Em 2021, é estimado 57 milhões de pessoas em todo o mundo Foi afetado pela demência, com a Alzheimer contribuindo em 60-70 % dos casos. Atualmente, não há cura para a doença de Alzheimer, mas há tratamentos que podem retardar os sintomas e melhorar a qualidade de vida.
Não é de surpreender que, na busca em andamento por respostas, os cientistas estejam cada vez mais voltando sua atenção dos neurônios para os vizinhos menos conhecidos, mas em pé de igualdade: as células imunológicas residem no cérebro.
Em novo Bilhete Postado em ImunidadeOs pesquisadores, liderados por Goraf Chopra na Universidade de Bordeaux, descobriram como o metabolismo da gordura em células pequenas da glia pode ser um dos principais fatores para o desenvolvimento da doença.
“Este estudo é amplamente interessante e parte de uma coleta crescente de estudos que indicam o papel dos problemas do metabolismo da gordura em células em torno de placas amilóides”, disse Deepak Nair.
Link para gordura
Em cérebros saudáveis, as pequenas células gliais atuam como células de vigilância, desinfetar resíduos e produtos proteicos tóxicos, como o beta -amilóide (Aβ), que é a molécula pegajosa que forma as características distintas das características da Alzheimer. Esse processo de limpeza ajuda a proteger os neurônios contra danos. Mas nos pacientes de Alzheimer, esse mecanismo falha.
“A grande questão era: como e por que as pequenas células gliais não são mais capazes de comer ou limpar essas pinturas?” Bri Brakash, autor do treinador do jornal, disse. “Esta não é uma nota nova. O próprio Dr. Al -Zheimer notou as lacunas gordas nas células gliais há mais de um século, mas sua importância funcional não estava clara até agora”.
O estudo DGAT2, uma enzima que transforma os ácidos graxos livres em uma tri -glicerina (marcas), o principal componente das gotas de gordura, como principal jogador. Nos modelos de camundongos e amostras de cérebro humano após a morte de pacientes com doença de Alzheimer no estágio final, os pesquisadores descobriram que pequenas células gliais próximas a placas amilóides têm uma alta expressão DGAT2 e inchadas com gotas de gordura, especialmente na área fortificada, responsável pela memória.
“Vemos que a proximidade de pequenas células gliais com as placas está relacionada ao tamanho das gotas de gordura. Quanto mais próximos elas se aproximam, mais elas as obtêm”, indicou Brakash.
O que faz com que o excesso de carga gorda? Segundo o estudo, a exposição Aβ leva à reação da cadeia metabólica. Pequenas células gliais começam a converter ácidos graxos livres em gorduras armazenadas em gotas de gordura. Com o tempo, esse acúmulo de gordura é interrompido por sua capacidade de despejar e digerir mais Aβ e coloca um ciclo vicioso: mais pinturas levam a mais gordura, o que leva a mais desequilíbrio.

A equipe de pesquisa utilizou fotografia avançada, análise sebácea e metabolismo para rastrear como alterar os arquivos de gordura de gordura para a gordura ao longo do tempo em resposta à exposição Aβ. Inicialmente, os pequenos, além dos ácidos graxos acumularam ácidos graxos tóxicos. Mais tarde, com a ajuda da enzima DGAT2, eles converteram esses ácidos graxos em um trio de glicerina e armazenados em gotas de gordura.
Para testar se esse acúmulo de gordura pode ser revertido, os pesquisadores usaram camundongos geneticamente engenharia que imitam os alzheimer humanos, conhecidos como camundongos 5xfad. Dois métodos foram utilizados para reduzir a atividade do DGAT2: um inibidor de medicamentos, atualmente em ensaios clínicos de doenças hepáticas gordurosas não alcoólicas e protaches especialmente semelhantes a direcionar especificamente DGAT2 especificamente em pequenas células gliais.
“Quando impedimos o DGAT2, vimos uma diminuição no acúmulo de gordura em células gliais pequenas e restaurar sua capacidade de remover placas amilóides. Mesmo o tratamento de uma semana em camundongos antigos com patologia pesada reduziu bastante a carga negra com mais de 50 % e sinais limitados de danos nervosos”, Prakash. “
No entanto, o professor Nair alertou que o modelo animal usado neste estudo é o modelo acelerado da doença de Alzheimer depende de doenças de Aβ e, portanto, os resultados podem não ser aplicáveis a todas as formas ou estágios da doença.
Quebra -cabeça cheio de filme
As gotas de gordura não são ruins de natureza. De fato, eles ajudam as células a sobreviver armazenando com segurança o excesso de gordura. Mas nas pequenas células gliais que são crônicas expostas ao Aβ, essa resposta de proteção se torna uma vez prejudicial. Os autores do estudo sugeriram que o sacrifício em pequenas células gliais nas funções de imunidade protetora em troca de segurança de gordura e que essa comparação pode ser uma etapa básica no progresso da doença de Alzheimer.
O estudo também revelou um sexo perceptível baseado em sexo: as camundongos fêmeas acumularam mais quedas de gordura nas células da glia pequenas e mostraram mais fraquezas graves do que os homens. Ele repetiu esses dados realistas que mostram às mulheres um Risco É desenvolvido pela Alzheimer.
Como o DGAT2 é expresso em muitos tipos de células em todo o corpo, seu direcionamento sistematicamente pode levar a efeitos colaterais indesejados. O artilheiro das células finas da equipe é um passo precoce, mas promissor, em direção à terapia celular seletiva.

“Esta é uma bela evidência do conceito”, disse o professor Nair. “Fomos expostos a mais de 100 propriedades nos ensaios clínicos da doença de Alzheimer nos últimos vinte anos e muito poucos tiveram sucesso. Esta doença é complicada em sua origem – não é o resultado de uma coisa”.
Enquanto a hipótese do amilóide dominou o campo por décadas, as teorias mais modernas incluem inflamação, o emaranhado da proteína tau, o desequilíbrio funcional metafísico e agora o metabolismo da gordura.
O professor Nair disse: “Em doenças cerebrais, o equilíbrio entra em colapso lentamente até que o sistema fique sobrecarregado”. “Se pudermos controlar três ou quatro caminhos críticos, o metabolismo da gordura é um deles, pode ser suficiente desacelerar esse colapso.
“E desacelerar. Um atraso de cinco anos no início do Alzheimer reduziria significativamente a carga social e econômica da doença”.
Manjeera Gowravaram possui doutorado em Bioquímica do RNA e trabalha como escritor de ciências independente.
Publicado 13 de julho de 2025 05:00




