O novo sistema pode explicar a resistência da terapia com carros no linfoma agressivo de células B
Crédito Chitraya Saar: Células cancerígenas (2025). Doi: 10.1016/j.ccell.2025.05.013
Uma equipe de pesquisa descobriu um mecanismo já desconhecido que pode sugerir que muitos pacientes com linfoma agressivo de células B não respondem à terapia celular CAR T há muito tempo. Os resultados do estudo sugerem que adicionar esse tratamento inovador com outros tratamentos pode melhorar ainda mais sua eficácia.
O trabalho está ligado Publicado No diário Células cancerígenas. A equipe de pesquisa é composta por pesquisadores da Faculdade de Hospital Universitário de Colon e Universidade de Colon, liderada pelo professor Dr. Roland é um médico sênior da Clínica I de Medicina Interna liderada por Ularich.
Nos últimos anos, a terapia de células CAR-T revolucionou pacientes com os chamados “recapsões ou r/r)”. Linfoma Protegendo a doença ou definido por um curso resistente à medicina. Esse processo envolve a alteração genética das próprias células T do paciente, para que elas possam identificar e destruir especificamente. CâncerAssim,
As células CAR-T direcionadas ao marcador de células B 19 se mostraram altamente eficazes e foram aprovadas em todo o mundo para o tratamento de pacientes que sofrem de linfoma agressivo de células B. No entanto, essa terapia é eficaz para cerca de metade dos pacientes a longo prazo.
Cerca de 50% dos pacientes tratados com células CAR-T não mostram uma resposta durável e, apesar do tratamento, não sofrem morrer ou morrer de sua doença. Existem muitas razões para isso, e mais pesquisas são necessárias neste campo.

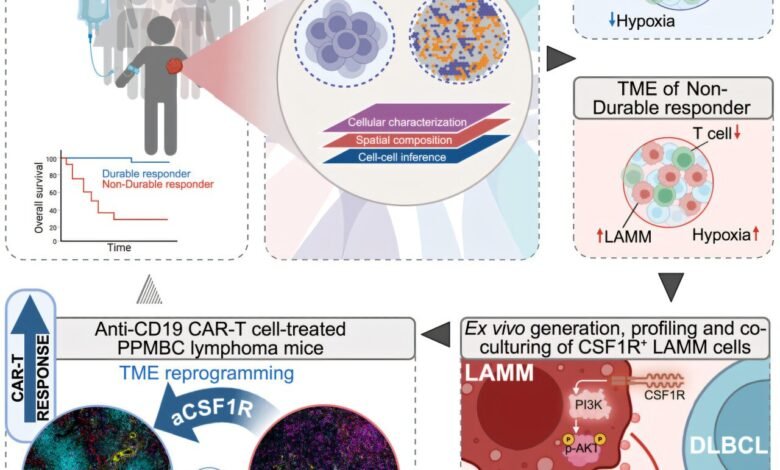
O perfil de proteínas de uma citometria agressiva de B-NHL (a) de imagem de imagem (IMC) de uma amostra agressiva de B-NHL. Barra de escala, 200μm. Crédito: Células cancerígenas (2025). Doi: 10.1016/j.ccell.2025.05.013
Para examinar essas perguntas não respondidas, a equipe de pesquisa do cólon, na qual o primeiro escritor do artigo, Dr. David Stall, Dr. Philip Godel e Dr. Hayat Balak-Vent, incluindo, analisaram as amostras do paciente antes e depois do tratamento de células-T usando métodos de biologia celular de última geração.
Os pesquisadores descobriram um tipo específico de célula imune, as chamadas células-monocíticas Mileoid CSF1R positivas (também conhecidas como células LAM), especialmente em pacientes, aumentaram sem uma reação durável. Ele demonstrou que essas células LAM estragam especialmente a função médica das células CAR-T contra o linfoma e, portanto, contribuindo para a falha da terapia celular CAR-T.
“Nossos resultados sugerem que essas células LAM atuam como um tipo de barreira, que protege os tumores das células CAR-T. Eles impedem os efeitos das células CAR-T, impedindo assim a eficácia da terapia celular CAR-T”, diz o professor Ularich, que é o último autor do estudo.
Aparentemente, o autor pode exibir em modelos de camundongos pré-price que a eficácia das células CAR-T é significativamente melhorada se as células LAM forem direcionadas usando o medicamento já aprovado, um inibidor de CSF1R. Esses achados são um passo importante em direção a uma nova terapia combinada, que inclui o uso de células CAR-T em associação com o inibidor do CSF1R.
O próximo passo é testar essa abordagem em um teste clínico com pacientes que sofrem de linfoma agressivo de células B.
Mais informações:
David Stall et al., CSF1RAssim, As células monocíticas myloides executam resistência às células car-T em linfoma agressivo de células B, Células cancerígenas (2025). Doi: 10.1016/j.ccell.2025.05.013
fornecido por
Universidade de Colon
Citação: O novo mecanismo pode explicar a resistência da terapia com carros no linfoma agressivo das células B (2025, 23 de junho). Em 23 de junho de 2025 https://medicalxpress.com/news/2025-06-06-06-06-06-06-06-racanismo-erapia-Therapy-sistância-fgressive.html
Este documento está sujeito a direitos autorais. Além de qualquer comportamento imparcial para fins de estudos ou pesquisas privadas, nenhuma parte pode ser retroduzida sem permissão por escrito. O conteúdo é fornecido apenas para fins de informação.




